La degenerazione maculare legata all’età (AMD) rappresenta una patologia degenerativa della macula, compromettendo la visione centrale. L’AMD è ampiamente riconosciuta come la principale causa di perdita di vista tra le persone anziane, poiché il processo di invecchiamento aumenta il rischio di sviluppare questa patologia. La sua prevalenza è in costante aumento a livello globale, richiamando l’attenzione sulla necessità di strategie preventive e trattamenti efficaci.
La malattia si manifesta in due forme principali: la secca, caratterizzata da depositi di materiale di scarto nella macula, e la umida, associata a vasi sanguigni anomali che possono causare danni rapidi.
In quest’ultimo caso si verifica la produzione di fluido, che determina un sollevamento della regione maculare con perdita acuta di vista. Nelle fasi avanzate della malattia, si verifica una progressiva perdita di cellule retiniche, quadro configurabile con il termine di atrofia.
Epidemiologia e fattori di rischio
L’epidemiologia della AMD rivela un notevole impatto sulla popolazione anziana. Questa condizione è particolarmente diffusa nei paesi industrializzati, dove l’aspettativa di vita è più elevata. Le stime indicano che la prevalenza di AMD aumenta significativamente con l’avanzare dell’età, con una maggiore incidenza tra gli individui oltre i 50 anni e un rischio significativamente aumentato dopo i 75 anni.
I fattori di rischio associati all’AMD includono l’invecchiamento stesso, la predisposizione genetica, il fumo, l’obesità e l’esposizione cronica alla luce ultravioletta. L’ereditarietà svolge un ruolo rilevante, con individui con antecedenti familiari di AMD che presentano un rischio più elevato di sviluppare la malattia. Le donne mostrano un’incidenza leggermente superiore rispetto agli uomini, mentre fattori come l’ipertensione arteriosa e una dieta povera di antiossidanti possono anche contribuire al rischio di sviluppare AMD. La comprensione approfondita di questi fattori di rischio è essenziale per sviluppare strategie preventive e trattamenti mirati, riducendo così l’onere globale della degenerazione maculare legata all’età sulla salute visiva della popolazione anziana.
Caratteristiche cliniche
La AMD presenta caratteristiche cliniche distintive che influenzano la visione centrale, spesso manifestandosi gradualmente. La forma secca, detta anche atrofica, è caratterizzata dalla presenza di depositi di detriti cellulari nella retina, note come drusen. Queste drusen, rappresentando uno stimolo pro-ossidante e degenerativo, possono portare a una perdita progressiva delle cellule fotosensibili nella macula, compromettendo la capacità di percepire i dettagli visivi. La presenza delle drusen configura il quadro di AMD precoce-intermedia. Le due forme che caratterizzano gli stadi avanzati sono la forma umida o essudativa, e la forma atrofica.
La forma umida, o neovascolare, comporta la crescita di vasi sanguigni anomali nel contesto della regione maculare. Questi vasi possono perdere sangue o liquidi, causando danni rapidi alla macula. I pazienti possono sperimentare distorsioni della visione, linee rette che sembrano curve, e una progressiva perdita della funzione visiva. I sintomi comuni includono la visione offuscata o distorta, difficoltà nella lettura e una diminuzione della capacità di riconoscere i dettagli fini. Nella forma umida il calo della vista è abbastanza repentino, anche se gli attuali trattamenti possono garantire un ottimo recupero visivo ed una buona gestione sul lungo periodo. La forma atrofica, invece, si caratterizza per una lenta e inevitabile perdita di cellule retiniche. Il calo della vista è lento e progressivo, e porta alla formazione di uno scotoma centrale, ovvero un buco nero al centro del campo visivo.
Caratteristiche di imaging
L’imaging è un aspetto cruciale nella diagnosi e nel monitoraggio della AMD, consentendo una valutazione dettagliata delle alterazioni nella regione maculare. Diverse tecniche di imaging forniscono informazioni preziose per comprendere la morfologia e il grado di coinvolgimento della malattia.
La tomografia ad ottica coerente (OCT) è uno strumento di imaging fondamentale nella valutazione dell’AMD. Questa tecnica consente di ottenere immagini ad alta risoluzione della retina, rivelando cambiamenti strutturali come l’ispessimento della retina, la presenza di fluidi, l’identificazione di membrane neovascolari e la perdita di tessuto retinico. L’OCT è una tecnica molto veloce e facilmente ripetibile, e rappresenta la pietra miliare per il monitoraggio dell’andamento della AMD.
La fluoresceina e l’angiografia con verde indocianina (FA e ICGA) sono utilizzate per studiare le caratteristiche vascolari della retina. La FA evidenzia le alterazioni dei vasi sanguigni attraverso l’iniezione endovena di fluoresceina sodica, mentre l’ICGA è più specifica per le strutture vascolari più profonde, come i vasi coroidei. Tali esami sono molto utili per evidenziare anomalie vascolari come la presenza delle neovascolarizzazioni maculari o la perdita di tessuto vascolare retinico. Una recente evoluzione dell’OCT, noto come angiografia OCT (OCTA), permette di ottenere informazioni molto dettagliate riguardanti la vascolarizzazione retinica, senza impiego di mezzo di contrasto. È per tale motivo che, sebbene non abbia soppiantato FA e ICGA, oggi OCTA rappresenta la metodica di diagnostica vascolare più facilmente ripetibile durante le visite.
Imaging a colori e autofluorescenza possono rivelare cambiamenti nelle cellule pigmentate della retina e nelle aree di accumulo di lipofuscina, contribuendo così a una valutazione più completa delle caratteristiche morfologiche dell’AMD, soprattutto focalizzandosi sulla progressiva perdita di tessuto (atrofia).
Trattamento
Il trattamento della AMD varia a seconda della forma della malattia: secca (atrofica) o umida (neovascolare).
Forma Secca (Atrofica): Attualmente, non esiste una cura definitiva per la forma secca dell’AMD. La forma precoce-intermedia trae giovamento dall’impiego di nutraceutici, ovvero sostanza di origine naturale (vitamine e minerali, acidi grassi omega3 e luteina), definiti dalla nota formulazione AREDS (Age-Related Eye Disease Study), in grado di ridurre la di progressione della malattia. Per le forme atrofiche avanzate si stanno affacciando nuovi potenziali trattamenti in grado di ridurre il tasso di progressione della perdita di tessuto. Tra le molecole più promettenti vi sono certamente gli inibitori del complemento. Il farmaco pegcetacoplan, somministrato per via intravitreale, ha dimostrato di ridurre del 20% il tasso di progressione dell’atrofia, ed è stato recentemente approvato per il trattamento della forma atrofica avanzata di AMD (atrofia geografica).
Forma Umida (Neovascolare): La forma umida dell’AMD richiede un trattamento più attivo. Le terapie anti-VEGF (fattore di crescita vascolare endoteliale) sono state rivoluzionarie. Iniezioni intravitreali di farmaci anti-VEGF, come ranibizumab, aflibercept o bevacizumab, sono somministrate per inibire la crescita dei vasi sanguigni anomali, riducendo il rischio di perdita della vista. Queste iniezioni richiedono somministrazioni periodiche durante l’arco della malattia. Si parte con una dose d’attacco di tre iniezioni a cadenza mensile, e poi si procede ad intervalli sempre maggiori, decisi sulla base della risposta della malattia al trattamento.
Figure
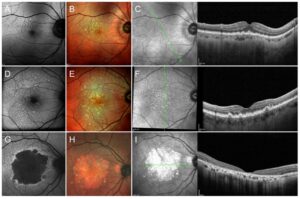
Figura 1: Stadi della AMD secca. Gli stadi più precoci di malattia si caratterizzano per la presenza di piccoli accumuli di materiale nella retina esterna. Questo materiale, meno evidenziabile dall’esame in autofluorescenza (A), risulta ben evidente sottoforma di accumuli giallognoli all’esame del fondo oculare (B). Quando tale materiale si localizza al disotto dell’epitelio pigmentato retinico, parliamo di drusen; quando al disopra, allora parliamo di pseudodrusen. L’esame OCT bene evidenzia la localizzazione di tali piccoli accumuli (C). Man mano che la malattia procede, gli accumuli di materiale diventano sempre più diffusi ed evidenti, come mostrato dall’esame in autofluorescenza (D) e dall’immagine a colori del fondo oculare (E). L’OCT rappresenta la metodica cardine per evidenziare e quantificare le drusen e pseudodrusen, che in questo caso configurano lo stadio di AMD intermedia (F). Lo stadio finale della forma secca è caratterizzato dalla comparsa di atrofia maculare (atrofia geografica). Questa risulta ben evidente in autofluorescenza, evidenziata come una regione ben delimitata ipoautofluorescente (scura) (G). Questa ben corrisponde all’area ipopigmentata evidenziata dall’immagine a colori del fondo oculare (H). L’OCT mostra un quadro di completa scomparsa (atrofia) degli strati retinici esterni, associata a marcata riduzione di spessore degli strati retinici interni (I).
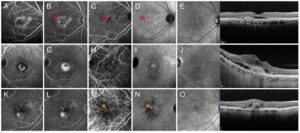
Figura 2: Forme di neovascolarizzazione maculare in AMD umida. La forma “occulta” (tipo 1) di neovascolarizzazione maculare (MNV) si caratterizza per un quadro aspecifico di rottura della barriera ematoretinica evidenziabile negli stadi precoci della fluorangiografia (A). La fase tardiva dell’esame mostra uno staining (riempimento) della lesione neovascolare (asterisco rosso) insieme a fenomeni di leakage (perdita di colorante) attorno alla lesione (B). L’esame in indocianina mostra già in fase precoce il network neovascolare (C) (asterisco rosso), maggiormente evidenziato nelle fasi tardive dell’esame (D). L’OCT conferma la presenza di una lesione neovascolare localizzata al disotto dell’epitelio pigmentato retinico, associata ad essudazione sottoretinica (E). La forma “classica” (tipo 2) di MNV si caratterizza per la comparsa della lesione neovascolare già negli stadi precoci della fluorangiografia (F). La fase tardiva dell’esame mostra un ulteriore staining (riempimento) della lesione neovascolare insieme a fenomeni di leakage (perdita di colorante) attorno alla lesione (G). L’esame in indocianina evidenzia già in fase precoce il network neovascolare (H), rimarcandone la presenza nelle fasi tardive dell’esame (I). L’OCT conferma la presenza di una lesione neovascolare localizzata al disopra dell’epitelio pigmentato retinico, associata ad essudazione sottoretinica ed intraretinica (J). La forma “proliferazione retinica angiomatosa” (tipo 3) di MNV non è ben evidenziabile dall’esame fluorangiografico (K,L). Spesso coesiste con MNV di tipo 1 o 2 che assumono le stesse caratteristiche fluorangiografiche sopra descritte. Al contrario, l’esame in indocianina è molto utile per evidenziare il piccolo spot ipercianescente già in fase precoce (asterisco arancione) (M), rimarcandone la presenza nelle fasi tardive dell’esame (N). L’OCT conferma la presenza di una lesione neovascolare intraretinica, associata a spots iperriflettenti ed essudazione intraretinica e sottoretinica (O).
DR
La retinopatia diabetica è una complicanza potenzialmente grave associata al diabete mellito, rappresentando una delle principali cause di cecità nei paesi industrializzati. Questa condizione colpisce la retina, e si sviluppa a seguito di cambiamenti vascolari (microangiopatia) e del tessuto nervoso (microneuropatia) causati dall’iperglicemia prolungata.
La retinopatia diabetica spesso progredisce senza sintomi evidenti nelle fasi iniziali, sottolineando l’importanza di esami oftalmologici regolari per la diagnosi precoce. La gestione della malattia può coinvolgere il controllo rigoroso della glicemia, la gestione della pressione sanguigna e, in alcuni casi, trattamenti laser o iniezioni intravitreali per prevenire o trattare le complicanze più gravi.
Epidemiologia e fattori di rischio
L’epidemiologia della retinopatia diabetica riflette l’ampia diffusione del diabete, sia di tipo 1 che di tipo 2. Con l’aumentare del numero di individui affetti da diabete, si registra una crescente incidenza di retinopatia diabetica, evidenziando l’urgenza di strategie di prevenzione e trattamento.
I fattori di rischio chiave includono il controllo inadeguato della glicemia, l’ipertensione arteriosa, la durata del diabete e i livelli elevati di lipidi nel sangue. I pazienti con diabete di lunga data sono più suscettibili allo sviluppo della retinopatia, specialmente se la gestione metabolica è inefficace. L’ipertensione contribuisce all’aggravamento della patologia, aumentando lo stress sui vasi sanguigni retinici.
La predisposizione genetica gioca anche un ruolo significativo, poiché alcuni individui sono più suscettibili a sviluppare complicanze oculari legate al diabete. La gestione adeguata dei fattori di rischio attraverso il monitoraggio regolare, il controllo della glicemia e la gestione della pressione sanguigna sono fondamentali per prevenire o ritardare la progressione della retinopatia diabetica. Un approccio multidisciplinare che coinvolge oftalmologi, endocrinologi e altri professionisti della salute è essenziale per una gestione completa della malattia.
Caratteristiche cliniche
La retinopatia diabetica è caratterizzata da una serie di alterazioni molto eterogenee della retina. Le caratteristiche cliniche di questa condizione possono variare in base alla fase della malattia, ma comprendono diversi elementi chiave.
- Microaneurismi e microemorragie: Nelle fasi iniziali, si presentano i microaneurismi, piccole dilatazioni dei vasi sanguigni retinici, che possono portare a sanguinamenti retinici. Questi fenomeni possono essere evidenti durante l’esame oftalmologico.
- Essudati: Lo spettro di essudati prevede diverse tipologie, ovvero essudati duri provenienti dalla fuoriuscita di sostanze attraverso la barriera ematoretinica danneggiata, e noduli cotonosi, provocati dall’accumulo di detriti neuronali all’interno dello strato delle fibre nervose.
- Edema Maculare: L’accumulo di liquido nella macula, l’area centrale della retina responsabile della visione nitida, causa il quadro di edema maculare. Ciò può comportare una visione offuscata o distorta, o un significativo calo dell’acuità visiva.
- Proliferazione Vascolare: In fasi più avanzate, la retinopatia diabetica può portare a una proliferazione anomala di nuovi vasi sanguigni, come abnormale risposta ai danni vascolari. Questi nuovi vasi, tuttavia, sono fragili e suscettibili di sanguinamenti, fino ad imponenti emorragie coinvolgenti l’intero spazio interno dell’occhio (emovitreo).
- Distacco della Retina: In casi avanzati, la retinopatia diabetica può contribuire al distacco della retina, causato dalle estese e demolitive proliferazioni fibrovascolari della retina, che può portare a una perdita permanente della vista.
La presenza di queste alterazioni consente la classificazione della retinopatia diabetica nei suoi diversi stadi, a gravità crescente: non proliferante, pre-proliferante e proliferante.
Caratteristiche di imaging
L’imaging della retinopatia diabetica svolge un ruolo fondamentale nella diagnosi, monitoraggio e gestione della malattia. Diverse tecniche di imaging forniscono informazioni dettagliate sulle alterazioni strutturali e vascolari della retina, consentendo una valutazione accurata del grado di severità e il piano di trattamento più adatto. La Fotografia del Fondo Oculare è uno strumento di base per la valutazione della retina. Queste immagini consentono di rilevare segni evidenti di retinopatia, come microaneurismi, sanguinamenti e alterazioni vascolari. La Tomografia ad Ottica Coerente (OCT) fornisce immagini dettagliate delle strutture retiniche interne ed esterne, permettendo la valutazione dello spessore della retina e di tutta una serie di biomarkers di grande utilità clinica, tra cui foci iperriflettenti (HF), disorganizzazione degli strati retinici interni (DRIL), eversione foveale, e molti altri. Questa tecnica è essenziale per monitorare la risposta ai trattamenti e la progressione della malattia. L’Angiografia con Fluoresceina (FA) rappresenta una tecnica fondamentale di imaging vascolare con mezzo di contrasto per evidenziare le anomalie vascolari della retina. L’FA è particolarmente utile per identificare le aree di rallentamento o perdita di flusso sanguigno (ischemia), sia a livello maculare che in periferia retinica. La più recente tecnica di angiografia OCT (OCTA) è in grado di fornire diverse utili informazioni riguardanti lo stato vascolare retinico. Tuttavia, permettendo uno studio dettagliato limitato alla sola regione centrale della retina, non è in grado di sostituire la FA per lo studio accurato della periferia.
Trattamento
Il trattamento della retinopatia diabetica mira a prevenire o limitare la progressione delle complicanze oculari associate al diabete. Le opzioni terapeutiche variano in base allo stadio della malattia e alle specifiche esigenze del paziente. Alcuni approcci chiave includono:
- Controllo Metabolico: Mantenere un controllo metabolico rigoroso della glicemia è fondamentale per prevenire e gestire la retinopatia diabetica. Il monitoraggio regolare della glicemia, unito a una dieta equilibrata e uno stile di vita sano, può contribuire a ridurre il rischio di complicanze oculari.
- Farmaci intravitreali Anti-VEGF e steroidei: Le iniezioni intravitreali di farmaci anti-VEGF (fattore di crescita vascolare endoteliale) o di corticosteroidi sono ampiamente utilizzate per il trattamento della retinopatia diabetica, in particolare nelle fasi caratterizzate da edema maculare e neovascolarizzazioni. Questi farmaci aiutano ad indurre il riassorbimento dell’edema maculare, a ridurre la crescita di nuovi vasi sanguigni e a prevenire il sanguinamento nella retina.
- Laserterapia: La fotocoagulazione laser può essere utilizzata per trattare aree specifiche della retina affette da ischemia. Questo contribuisce a ridurre gli stimoli per la crescita dei nuovi vasi sanguigni e per la ricomparsa di edema maculare.
- Chirurgia Vitreoretinica: In casi più gravi con trazioni vitreoretiniche e distacco della retina, la chirurgia vitreoretinica rappresenta l’opzione di scelta per ripristinare la normale anatomia della retina.
La scelta del trattamento dipende dalla gravità della retinopatia diabetica e dalla presenza di specifiche complicanze. La gestione della malattia richiede una collaborazione stretta tra oftalmologi, diabetologi e altri professionisti della salute per garantire un approccio completo e personalizzato. L’importanza del monitoraggio regolare e della diagnosi precoce è cruciale per preservare la vista nei pazienti con retinopatia diabetica.
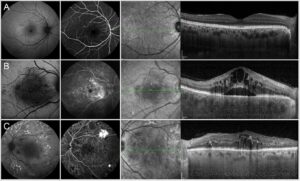
Figura: Stadi della retinopatia diabetica. Il primo caso (A) mostra uno stadio precoce di retinopatia diabetica, caratterizzato da modeste alterazioni del fondo oculare, come mostrato dall’esame in autofluorescenza. In fluorangiografia si evidenziano piccoli spots iperfluorescenti, compatibili con microaneurismi. Il quadro OCT è pressoché nei limiti di norma. Il secondo caso (B) mostra un quadro di retinopatia diabetica non proliferante complicato da edema maculare. L’esame in autofluorescenza mostra numerosi fenomeni di mascheramento del segnale, compatibili con microemorragie, essudati e con la presenza dell’edema maculare. L’esame fluorangiografico mostra una estesa rottura della barriera ematoretinica. L’OCT mostra chiaramente un imponente edema maculare, caratterizzato dal fluido sottoretinico ed intraretinico. Lo stadio più avanzato è rappresentato dalla retinopatia diabetica proliferante (C). In tal caso, è possibile riscontrare diffuse alterazioni a carico del polo posteriore, ma l’alterazione più evidente è la grossa lesione iperfluorescente riscontrabile in fluorangiografia, compatibile con una lesione proliferante neovascolare. L’OCT mostra inoltre il quadro di edema maculare con associati numerosi microessudati e fenomeni di disorganizzazione degli strati retinici interni, tutti biomarkers prognostici sfavorevoli della retinopatia diabetica.